Katalýza v organické chemii
Homogenní katalýza
- Wilkinsonův katayzátor
- je to komplex $[RhCl(PPh_3)_3]$
- analogický je Vaskův komplex $[IrCl(CO)(PPh_3)_2]$
- používá se při katalýze oxidačních procesů
- při hydrogenaci alkenů se používá schopnost $Rh^I$ vytvářet hydridokomplexy s elementárním vodíkem a koordinovat alkeny pomocí $\pi$-vazby
Mechanismus hydrogenace
- Wilkinsonův katalyzátor má planární strukturu odpovídající hybridizaci $sp^2d$
- jeden orbital $p$ je vakantní a umožňuje vstup další částice a případnou substituci ligandu a přestup na oktaedrickou koordinaci
- katalýza je zahájena substitucí jednoho trifenylfosfinového ligandu ligandem rozpouštědla
- tato reakce je reverzibilní
- rozpouštědlem je často benzen
- prvním krokem je vytvoření hydridokomplexu a přechod na oktaedr
- v druhém kroku dochází k substituci ligandu rozpouštědla za nespecificky vázaný alken
- dále probíhají přesmyky a postupně se oba koordinované vodíkové atomy naváží na alken
- dojde ke změně $\pi$-vazby alkenu na obyčejnou $\sigma$-vazbu
- uvolní se alkan
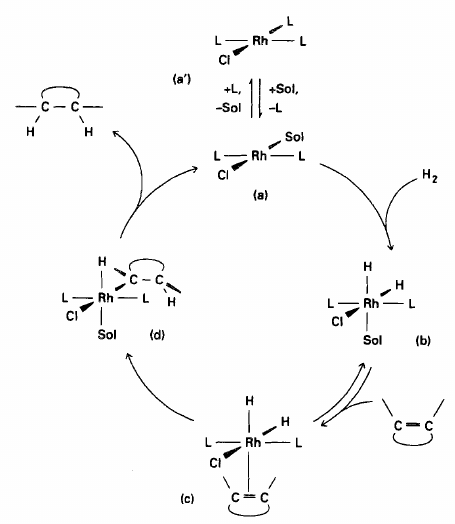
- $L$ - $PPh_3$
- $Sol$ - ligand rozpouštědla
- podobný proces nastává při hydroformylaci
- používá se obdobný komplex $[Rh(CO)(PPh_3)_3]$
Oxidace alkenů (Wackerův proces)
- jako katalyzátor se používá cholord palladnatý $PdCl_2$
Mechanismus oxidace alkenů
- v první části se palladium redukuje na komplex $Pd^0$
- charakter komplexu je málo prozkoumaný
- zpětná reakce je katalyzována chloridem měďnatým $CuCl_2$
- v nadbytku chloridů tvoří komplex $[CuCl_4]^{2-}$
- regenerace probíhá takto:
- $Pd^0+2\ [CuCl_4]^{2-}\longrightarrow{Pd^{2+}+2\ [CuCl_2]^-+4\ Cl^-}$
- $2\ [CuCl_2]^-+\frac{1}{2}O_2+2\ H^++4\ Cl^-\longrightarrow{2\ [CuCl_4]^{2-}+H_2O}$
- v dalším korku dochází k nespecifické koordinaci alkenu na $Pd^{II}$
- hydrolýzou vzniklého komplexu vzniká alkohol
- v následujícím koku dojde ke vzniku hydridokomplexu a předání vodíkového atomu molekule alkenu
- vzniklý aldehyd se uvolní kyselinou
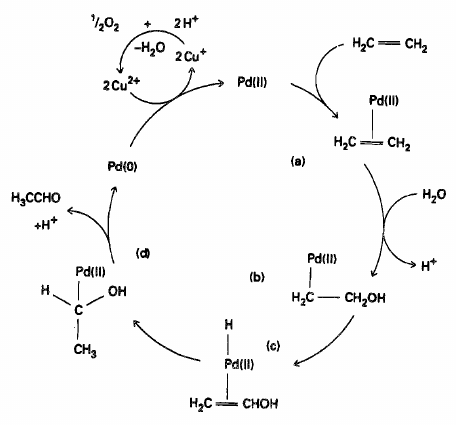
Polymerace alkenů
- Zieglerův-Nattův katalyzátor
- je to směs chloridu titaničitého a trialkylaluminia $AlEt_3$
- umožňuje provádět polymeraci za normální teploty
Mechanismus polymerace alkenů
- reakcí složek katalyzártoru vzniká komplex $TiCl_3Et$
- na komplex se $\pi$-vazbou koordinuje alken
- tato vazba je velmi nestálá a proto dochází přesmyku na vazbu $\sigma$ a inzerci alkenu mezi atomy titanu a již vázaný alkyl
- tento děj se neustále opakuje
Heterogenní katalýza
Hydrogenace nenasycených uhlovodíků
- nejčastěji probíhá na povrchu niklu elementárním vodíkem
- jako hydrogenační činidlo se používá často deuterium
- činidlo i molekula olefinu se adsorbují na povrch kovu
- sorbované molekuly migrují po povrchu
- pokud se molekuly k sobě dost přiblíží, dojde k reakci
- na závěr se oddělí molekula alkanu

