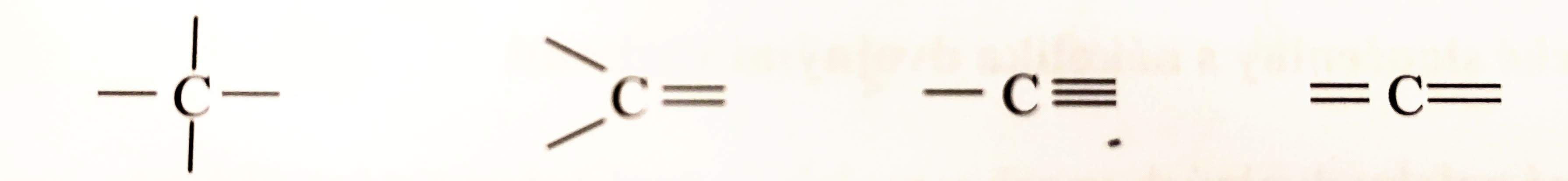Chemické vazby v organických sloučeninách
Vaznost prvků v organických sloučeninách
- v organických sloučeninách má každý prvek danou vaznost
- Uhlík
- je vždy čtyřvazný
- může tvořít jednoduchou, dovjnou i trojnou vazbu
- čím je vazba násobnější, tím je pevnější a kratší
- nejpevnější je vazba trojná
- ma největší disociační energii
- hovoříme o fyzikální stabilitě
- jednoduché vazby jsou méně reaktivní
- hovoříme o chemické stabilitě
- je vždy v excitovaném stavu ($_6C^*:[_2He]2s^12p^3$)
- Dusík
- je trojvazný
- může tvořit jednoduché a trojné vazby
- Kyslík
- je vždy dvojvazný
- muže tvořit jednoduché a dovjné vazby
- Síra
- je buď dvojvazná, čtyřvazná nebo šestivazná
- dvojvazná třeba ve skupině $-SH$
- čtyřvazná třeba ve skupině $>S=O$
- šestivazná třeba ve skupině $-SO_{3}H$
- Halogeny
- jsou vždy jednovazné
- tvoří pouze jednoduché vazby
- Vodík
- je vždy jednovazný
- tvoří pouze jednoduché vazby
- $sp^{3}$ hybridizaci odpovídá atom uhlíku, ze kterého vycházejí čtyři $\sigma$-vazby
- molekuly má tvar tetraedru
- např. methan ($CH_{4}$)
- $sp^{2}$ hybridizaci odpovídá atom uhlíku, ze kterého vychází tři vazby $\sigma$ a jedna vazba $\pi$
- z uhlíku tedy vychází dvě jednoduché vazby a jedna dvojná vazba ($>C=$)
- např. ethen ($H_{2}C=CH_{2}$)
- $sp$ hybridizaci odpovídá atom uhlíku, ze kterého vychází dvě vazby $\sigma$ a dvě vazby $\pi$
- z uhlíku tedy vychází dvě dvojné vazby nebo jedna jednoduchá a jedna trojná vazba
- např.: ethyn $HC\equiv{CH}$
Zásady strukturní teorie organických sloučenin
- Uhlík je vždy čtyřvazný
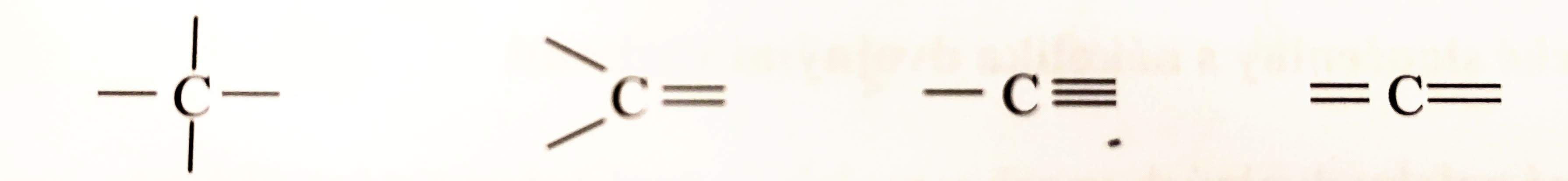
- Vazby uhlíku jsou vždy rovnocené
- Vazby v nasycených sloučeninách svírají vždy úhel 109°
- všechny atomy uhlíku v takové sloučenině mají hybridizaci $sp^{3}$
- Sloučeniny s dvojnou vazbou jsou v místě této vazby planární a vždy svírají úhel 120°
- atomy uhlíku s vatbou $C=C$ jsou v jedné rovině
- atomy uhlíku spostředkovávající tuto vazbu mají hybridizaci $sp^{2}$
- Sloučeniny s trojnou vazbou jsou v místě této vazby lineární a vždy svírají úhel 180°
- atomy uhlíku tvořící trojnou vazbu mají hybridizaci $sp$
- Pouze jednoduché vazby jsou volně otáčivé
- otáčením skupiny atomů kolem jednoduchých vazeb vznikají konformery
- někdy je rotace těchto skupin omezena prostorem
- platí to jak pro řetězcovité sloučniny, tak pro cyckly
- násobné vazby otáčivé nejsou
- Každá sloučenina má snahu zaujímat nejvýhodnější konformaci
- nevazebné interakce v takovém stavu jsou v molekule minimální
- skupiny a atomy jsou maximálně daleko od sebe
- Vlastnosti organických sloučenin závisí na jejich struktuře
- se znalostí struktury lze vlastnost organických sloučeniny předpovídat
Organické sloučeniny s několika dvojnými vazbami
- rozlišujeme tři vzájemné polohy dvojných vazeb
- Kumolované dvojné vazby
- dvě dvojné vazby jsou vedle sebe
- z jednoho uhlíku vycházejí dvě dvojné vazby
- $=C=$
- Konjugované dvojné vazby
- dvě dvojné vazby jsou od sebe odděleny jednou jednoduchou vazbou
- $=C-C=$
- Izolované dvojné vazby
- mezi dvěma dvojnými vazbami jsou alespoň dvě jednoduché vazby
- $=C-C-C=$