Poznámky
• Chemie • Periodická tabulka • Anorganická chemie • Obecná anorganická chemie • Organická chemie • Obecná organická chemie • Základy společenských věd Karboxylové kyseliny
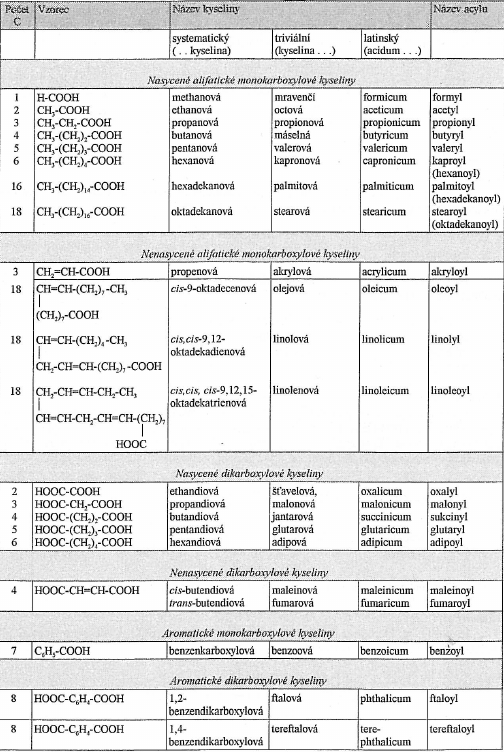
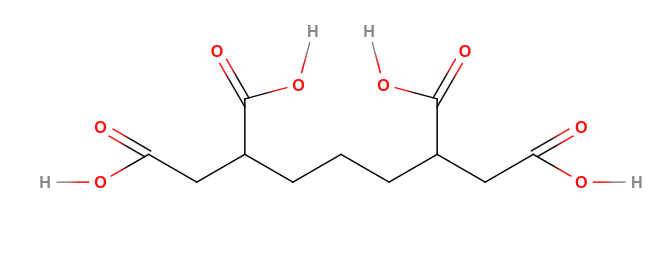
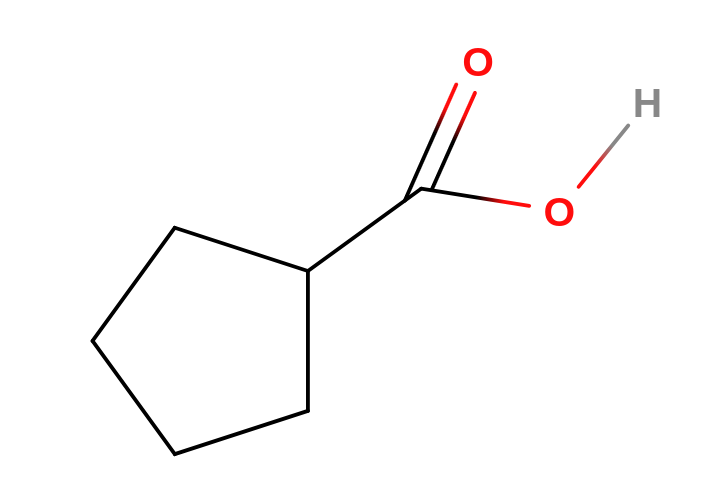
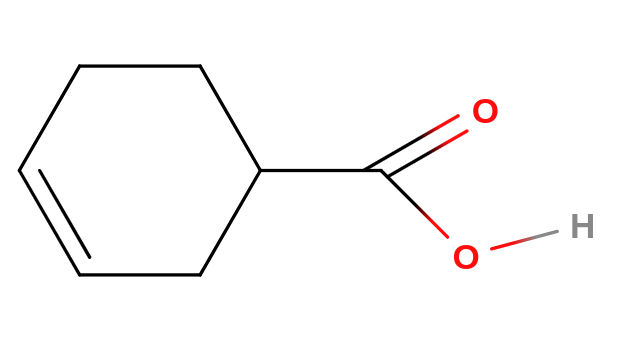
jsou to sloučeniny, které obsahují karboxylovou funkční skupinu ($-COOH$)obsahuje karbonylovou skupinu ($-C=O$) a hydroxyskupinu ($-OH$) obecný vzorec: $R-COOH$ ve vodě disociují a odštěpují proton jsou slabé, ale silnější než kyselina uhličitá Dělení karboxylových kyselin Podle počtu karboxylových skupin monokarboxylové jedna karboxylová skupina dikarboxylové polykarboxalové více karboxylových skupin Podle typu řetězce Nomenklatura karboxylových kyselin Substituční název Alicyklické karboxylové kyseliny název z celkového počtu uhlíků + suffix -ová a slovo kyselina karboxylová skupina má nejvyšší prioritu pokud se nachází karboxylové skupiny na uhlících, které nelze zařadit do hlavního řetězce, odstraníme je všechny z původního uhlovodíku a přidáme suffix -karboxylová např.:$HCOOH$ - methanová kyselina $CH_2=CH-COOH$ - prop-2-enová kyselina $HOOC-CH_2-COOH$ - propan-1,3-diová kyselina hexan-1,2,6,7-tetrakarboxylová kyselina Cyklické karboxylové kyseliny název podle cyklu + suffix -karboxylová a slovo kyselina např.:cyklopentankarboxylová kyselina cyklohex-3-enkarboxylová kyselina Triviální název bývá založený na objektu, ze kterého byla poprvé izolována Názvy vybraných kyselin a jejich acylů Příprava karboxylových kyselin některé kyseliny se získávají z přírodních zdrojů Oxidace alkanů průmyslově se výrabí oxidací těžších alkanů ($C_{20}$ - $C_{30}$) vzdušným kyslíkem při této metodě vznikají různé vedlejší produkty (alkoholy, ketony) ze směsi se izolují ve formě sodných solí, které se okyselí Oxidace roztokem manganistanu draselného Alkeny řetězec se rozštěpí v místě dvojné vazby vznikají dvě raselné soli kyseliny se získají jejich okyselením Areny oxiduje se postranní řetězec aromatické sloučeniny dříve se tak vyráběla kyselina benzoová nebo kyselina tereftalová Alkoholy a aldehydyv první fázi vzniká aldehyd oxidací aldehydu vzniká kyselina Katalytická oxidace arenu v první fázi vzniká anhydrid ve vodném prostředí hydrolyzuje a poskytuje kyselinu Fyzikální vlastnosti karboxylových kyselin nižší alifatické monokarboxylové kyseliny jsou kapaliny vyšší alifatické karboxylové kyseliny jsou pevné krystalické látky dikarboxylové a aromatické kyseliny jsou pevné krystalické látky bod varu roste s molekulovou hmotností mezi molekulami karboxylových kyselin se tvoří vodíkové můstky v plynném stavu se mohou vyskytovat jako dimery s délkou uhlovodíkového řetězce klesá rozpustnost ve vodě nižší monokarboxylové kyseliny většninou silně zapáchají vyšší karboxylové kyseliny jsou prakticky bez zápachu Chemické vlastnosti karboxylových kyselin Karboxylová skupina kyslík navýzaný dvojnou vazbou způsobuje parciální kladný náboj na karboxylovém uhlíku kladným parciálním nábojem se zvyšuje polarizovatelnost vazby $O-H$ vazba se snadno štěpí karboxylové kyseliny jsou proto o něco silnějšími kyselinamihodnota konstanty acidity se pohybuje v rozmezí $10^{-4}$ až $10^{-5}$ sílu kyseliny snižují uhlovodíkové substituenty sílu kyselin zvyšují substituenty s -I efekterm a násobné vazby blízko k funkční skupině Reakce karboxylových kyselin Neutralizace vznikají soli karboxylových kyselin a vody soli snadno hydrolizují bůsobením silných anorganických kyselin se ze solí uvolnují karboxylové kyseliny Esterifikace je to reversibilní reakce karboxylové kyseliny a alkoholu zpětná rekace se nazývá kyselá hydrolýza esterů vzniká ester a voda probíhá za přítomnosti katalytického množství silné kyseliny experimentálně bylo zjištěno, že voda vznkne odštěpením hydroxyskupiny z karboxylové kyseliny a vodíku z hydroxyskupiny alkoholu Dekarboxylace z karboxylové skupiny se odštěpí oxid uhličitý řetězec produktu je o jeden uhlík kratší Dehydratace probíhá účinkem činidel vznikají anhydridy Zástupci Kyselina mravenčí $HCOOH$, kyselina methanová, acidum formicum nachází se v jedu mravenců a vos a v listech kopřiv průmyslově se vyrábí oxidací methanolu je to bezbarvá ostře zapchající látka používá se ke konzervaci, při barvení a jako baktericid používá se při zpracování kůže Kyselina octová $CH_3COOH$, kyselina ethanová, acidum aceticum je to čirá kapalina štiplavého zápachu vyrábí se octovým kvašením lihových roztoků nebo oxidací acetaldehydu běžně se prodává ve formě 8% roztoku používá se k výrobě acetátového hedvábí a konzervaci používá se při výrobě některých léků octan hlinitý (aluminium-triacetát ) se používal k přípravě obkladů na otokyKyselina máselná $CH_3CH_2CH_2COOH$, kyselina butanová, acidum butyricum vyznačuje se velmi nepříjemným zápachem ve formě sesteru je obsažena v másle uvolňuje se při žluknutí másla Vyšší mastné kyseliny většina je obsaženy v tucích soli některých z nich se používají v mýdlech kyselina palmitová kyselina steraová kyselina olejová kyselina eladová kyselina linolová kyselina linolenová Kyselina benzoová $C_6H_5-COOH$, kyselina benzenkarboxylová, acidum benzoicum používá se ke konzervaci a v organické syntéze v přírodě se vyskytuje ve formě esterů Kyselina šťavelová $(COOH)_2$, kyselina ethandiová, kyselina oxalová, acidum oxalicum vyskytuje se v rostlinách ve formě solí je jedovatápoužívá se k přípravě mořidel v analytické chemii se používá jako standard Kyselina adipová $HOOC-(CH_2)_4-COOH$, kyselina hexandiová, acidum adipicum používá se k výrobě Nylonu Kyselina ftalová $HOOC-C_6H_4-COOH$, kyselina benzen-1,2-dikarboxylová, acidum phtalaicum tvoří bílé destičkové krystaly její anhydrid je výchozí látkou pro výrobu barviv a indikátorů kyselina tereftalová (kyselina benzen-1,4-dikarboxylová ) je jejím izomerempoužívá se k výrobě umělých vláken (trevíra, tesil, terylen )